新スクリーニング法 HaiDap を開発し、細胞ベース試験との“橋渡し”に成功
室蘭工業大学大学院工学研究科の倉賀野正弘助教と徳樂清孝教授および株式会社カネカ再⽣・細胞医療研究所の⻄下直希博⼠らの研究グループ※1は、アルツハイマー病の原因と考えられるアミロイドβ(Aβ)の凝集を阻害する素材を、患者由来iPS細胞から分化させた神経細胞の培養上清を用いて迅速・低コストに評価できる新しいスクリーニング手法 HaiDapを開発しました。従来のin vitro 試験とiPS細胞ベース試験の結果のズレを埋める「中間評価系」として機能し、創薬初期段階の実効性検証を加速することが期待されます。
この研究成果は、令和8年3月24日に、国際学術雑誌「Nature Communications」に掲載されました。
研究のポイント
・患者由来iPS神経細胞の培養上清中でAβ凝集阻害活性を評価することで、アルツハイマー病の予防や治療への効果が期待されるAβ凝集阻害物質を、少量・省コストで効率的に探索する新手法HaiDap(High‑throughput screening technology for Aggregation Inhibitors of Diseased cell‑derived Aggregative Proteins)を確立。
・tau、α-シヌクレイン、Serum Amyloid Aなど、様々な疾患(パーキンソン病、AAアミロイドーシスなど)の発症に関与する他の凝集性タンパク質へも展開可能。
・22種の植物抽出物を評価し、Orthosiphon aristatus (ネコノヒゲ)、Syzygium aromaticum (チョウジ)、Geranium yesoense (エゾフウロ)の3種がHaiDapとiPS細胞ベース試験の両方で有効と確認。
研究の背景
創薬初期では多くが試験管内(in vitro)でスクリーニングされますが、そこで選ばれた化合物が細胞・生体では効かないことが少なくありません。患者由来iPS細胞を用いる試験系は有望な一方、時間・コスト負担が大きく、多数候補の評価には不向きでした。さらに、培地添加物のアルブミンがAβ凝集を強く抑制してしまい、凝集阻害活性の正確な判定を妨げることが課題でした。
研究の内容
本研究では、室蘭工業大学が開発した量子ドット(QD)によるAβ凝集過程の可視化法を応用したタンパク質凝集抑制物質の微量ハイスループットスクリーニングシステム(特許第7166612号、PCT/JP2019/51077)と、株式会社カネカ 再生・細胞医療研究所のiPS細胞培養技術を組み合わせ、患者iPS細胞から分化誘導した神経細胞の培養上清中で凝集阻害物質をスクリーニングする新たなスクリーニング手法 High‑throughput screening technology for Aggregation Inhibitors of Diseased cell‑derived Aggregative Proteins (HaiDap)を開発しました。
【画像: (リンク ») 】
QDによるAβ凝集過程の可視化法のイメージ
【画像: (リンク ») 】
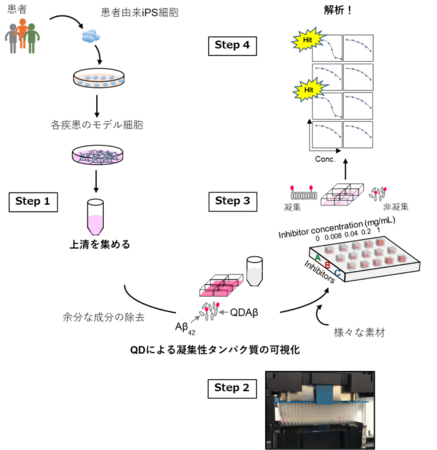
培養上清を用いたAβ凝集阻害素材の探索の概念図
Aβは、一般的な実験で用いられる生理的塩濃度の溶液(PBS)よりも培養上清中で早期に凝集開始し(PBS約4時間、培養上清約2時間)、細胞分泌由来の低分子やAβオリゴマーが凝集促進に寄与することを示しました。
【画像: (リンク ») 】
培養上清中でのAβ凝集の促進
さらに、自動化MSHTSと組み合わせて22種の植物抽出物を評価。3種(O. aristatus、 S. aromaticum、G. yesoense)はHaiDapで有効で、iPS細胞ベースの生細胞試験でもAβ凝集抑制を再現しました。 本手法は、アルツハイマー病の原因と考えられるAβに限らず、タウ、α-シヌクレイン、Serum amyloid Aなど他の凝集性タンパクの凝集可視化にも適用可能であることが確認できました。
今後の展開
・患者・疾患サブタイプごとの培養上清を用いた個別化スクリーニング(オーダーメイド創薬)への展開
【画像: (リンク ») 】
・αシヌクレインやtau、Serum amyloid Aなど病態関連分子を含む環境での疾患横断的評価系としての拡張。
・動物実験前の効率的な絞り込みにより、開発コスト・期間のさらなる短縮に貢献
論文情報
論文名:A high-throughput conditioned-media-based screening system identifies inhibitors of aggregation induced by iPSC-secreted amyloid β
雑誌名:Nature Communications
著者名:Masahiro Kuragano, Naoki Nishishita, Koki Araya, Akira Kobayashi, Taro Q.P. Noguchi, Kenichi Watanabe, Shinya Watanabe, Stefan Baar, Koji Uwai, Kiyotaka Tokuraku
D O I : (リンク »)
備考
※1 研究グループ構成員
室蘭工業大学 大学院工学研究科 化学生物工学ユニット倉賀野正弘 助教、徳樂清孝 教授、上井幸司 准教授、博士前期課程2年 荒谷康貴 氏、室蘭工業大学 大学院工学研究科 システム情報学ユニット 渡邉真也 教授、Stefan Baar 博士、株式会社カネカ 再生・細胞医療研究所 西下直希 博士、小林明 氏、都城工業高等専門学校 物質工学科 野口太郎 教授、帯広畜産大学 グローバルアグロメディシン研究センター 渡邉謙一 准教授
用語解説
・アミロイドβ(Aβ):アルツハイマー病で脳内に異常凝集・沈着するタンパク質断片。
・量子ドット(QD):蛍光性半導体ナノ結晶。タンパク質凝集のリアルタイム可視化に
利用。
・α-シヌクレインは:パーキンソン病に関連する病原性タンパク質。α-シヌクレインの
異常な凝集と蓄積は神経細胞死を引き起こす。
・EC50:半数効果濃度。値が小さいほど強い抑制活性を示す指標。
・iPS細胞:体細胞から作製した多能性幹細胞。患者由来細胞で疾患モデルを作成可能。
・Serum amyloid A:炎症によって肝臓から生成される血中タンパク質。AAアミロイドー
シスの原因としても知られている。
・tau:タウは微小管結合タンパク質。アルツハイマー病患者の脳において凝集し、神経原
線維変化(NFT)を形成する。アルツハイマー病のほか、タウオパチーと呼ばれる神経
変性疾患でも観察される。
謝辞
本研究はJSPS科研費 JP24K08627(K.T.)、JST 共創の場形成支援プログラム(COI-NEXT)JPMJPF2213(K.T.)の支援を受けました。TEM観察は文部科学省「ARIM」の支援を受け実施しました(課題番号 JPMXP1222CT0078)。
研究に関する問い合わせ
室蘭工業大学 大学院工学研究科 教授・クリエイティブコラボレーションセンター長
徳樂 清孝
E-mail:tokuraku@muroran-it.ac.jp mailto:tokuraku@muroran-it.ac.jp
報道に関する問い合わせ
国立大学法人室蘭工業大学総務広報課秘書広報係
Tel:0143-46-5008
E-mail:koho@muroran-it.ac.jp mailto:koho@muroran-it.ac.jp
室蘭工業大学大学院工学研究科の倉賀野正弘助教と徳樂清孝教授および株式会社カネカ再⽣・細胞医療研究所の⻄下直希博⼠らの研究グループ※1は、アルツハイマー病の原因と考えられるアミロイドβ(Aβ)の凝集を阻害する素材を、患者由来iPS細胞から分化させた神経細胞の培養上清を用いて迅速・低コストに評価できる新しいスクリーニング手法 HaiDapを開発しました。従来のin vitro 試験とiPS細胞ベース試験の結果のズレを埋める「中間評価系」として機能し、創薬初期段階の実効性検証を加速することが期待されます。
この研究成果は、令和8年3月24日に、国際学術雑誌「Nature Communications」に掲載されました。
研究のポイント
・患者由来iPS神経細胞の培養上清中でAβ凝集阻害活性を評価することで、アルツハイマー病の予防や治療への効果が期待されるAβ凝集阻害物質を、少量・省コストで効率的に探索する新手法HaiDap(High‑throughput screening technology for Aggregation Inhibitors of Diseased cell‑derived Aggregative Proteins)を確立。
・tau、α-シヌクレイン、Serum Amyloid Aなど、様々な疾患(パーキンソン病、AAアミロイドーシスなど)の発症に関与する他の凝集性タンパク質へも展開可能。
・22種の植物抽出物を評価し、Orthosiphon aristatus (ネコノヒゲ)、Syzygium aromaticum (チョウジ)、Geranium yesoense (エゾフウロ)の3種がHaiDapとiPS細胞ベース試験の両方で有効と確認。
研究の背景
創薬初期では多くが試験管内(in vitro)でスクリーニングされますが、そこで選ばれた化合物が細胞・生体では効かないことが少なくありません。患者由来iPS細胞を用いる試験系は有望な一方、時間・コスト負担が大きく、多数候補の評価には不向きでした。さらに、培地添加物のアルブミンがAβ凝集を強く抑制してしまい、凝集阻害活性の正確な判定を妨げることが課題でした。
研究の内容
本研究では、室蘭工業大学が開発した量子ドット(QD)によるAβ凝集過程の可視化法を応用したタンパク質凝集抑制物質の微量ハイスループットスクリーニングシステム(特許第7166612号、PCT/JP2019/51077)と、株式会社カネカ 再生・細胞医療研究所のiPS細胞培養技術を組み合わせ、患者iPS細胞から分化誘導した神経細胞の培養上清中で凝集阻害物質をスクリーニングする新たなスクリーニング手法 High‑throughput screening technology for Aggregation Inhibitors of Diseased cell‑derived Aggregative Proteins (HaiDap)を開発しました。
【画像: (リンク ») 】
QDによるAβ凝集過程の可視化法のイメージ
【画像: (リンク ») 】
培養上清を用いたAβ凝集阻害素材の探索の概念図
Aβは、一般的な実験で用いられる生理的塩濃度の溶液(PBS)よりも培養上清中で早期に凝集開始し(PBS約4時間、培養上清約2時間)、細胞分泌由来の低分子やAβオリゴマーが凝集促進に寄与することを示しました。
【画像: (リンク ») 】
培養上清中でのAβ凝集の促進
さらに、自動化MSHTSと組み合わせて22種の植物抽出物を評価。3種(O. aristatus、 S. aromaticum、G. yesoense)はHaiDapで有効で、iPS細胞ベースの生細胞試験でもAβ凝集抑制を再現しました。 本手法は、アルツハイマー病の原因と考えられるAβに限らず、タウ、α-シヌクレイン、Serum amyloid Aなど他の凝集性タンパクの凝集可視化にも適用可能であることが確認できました。
今後の展開
・患者・疾患サブタイプごとの培養上清を用いた個別化スクリーニング(オーダーメイド創薬)への展開
【画像: (リンク ») 】
・αシヌクレインやtau、Serum amyloid Aなど病態関連分子を含む環境での疾患横断的評価系としての拡張。
・動物実験前の効率的な絞り込みにより、開発コスト・期間のさらなる短縮に貢献
論文情報
論文名:A high-throughput conditioned-media-based screening system identifies inhibitors of aggregation induced by iPSC-secreted amyloid β
雑誌名:Nature Communications
著者名:Masahiro Kuragano, Naoki Nishishita, Koki Araya, Akira Kobayashi, Taro Q.P. Noguchi, Kenichi Watanabe, Shinya Watanabe, Stefan Baar, Koji Uwai, Kiyotaka Tokuraku
D O I : (リンク »)
備考
※1 研究グループ構成員
室蘭工業大学 大学院工学研究科 化学生物工学ユニット倉賀野正弘 助教、徳樂清孝 教授、上井幸司 准教授、博士前期課程2年 荒谷康貴 氏、室蘭工業大学 大学院工学研究科 システム情報学ユニット 渡邉真也 教授、Stefan Baar 博士、株式会社カネカ 再生・細胞医療研究所 西下直希 博士、小林明 氏、都城工業高等専門学校 物質工学科 野口太郎 教授、帯広畜産大学 グローバルアグロメディシン研究センター 渡邉謙一 准教授
用語解説
・アミロイドβ(Aβ):アルツハイマー病で脳内に異常凝集・沈着するタンパク質断片。
・量子ドット(QD):蛍光性半導体ナノ結晶。タンパク質凝集のリアルタイム可視化に
利用。
・α-シヌクレインは:パーキンソン病に関連する病原性タンパク質。α-シヌクレインの
異常な凝集と蓄積は神経細胞死を引き起こす。
・EC50:半数効果濃度。値が小さいほど強い抑制活性を示す指標。
・iPS細胞:体細胞から作製した多能性幹細胞。患者由来細胞で疾患モデルを作成可能。
・Serum amyloid A:炎症によって肝臓から生成される血中タンパク質。AAアミロイドー
シスの原因としても知られている。
・tau:タウは微小管結合タンパク質。アルツハイマー病患者の脳において凝集し、神経原
線維変化(NFT)を形成する。アルツハイマー病のほか、タウオパチーと呼ばれる神経
変性疾患でも観察される。
謝辞
本研究はJSPS科研費 JP24K08627(K.T.)、JST 共創の場形成支援プログラム(COI-NEXT)JPMJPF2213(K.T.)の支援を受けました。TEM観察は文部科学省「ARIM」の支援を受け実施しました(課題番号 JPMXP1222CT0078)。
研究に関する問い合わせ
室蘭工業大学 大学院工学研究科 教授・クリエイティブコラボレーションセンター長
徳樂 清孝
E-mail:tokuraku@muroran-it.ac.jp mailto:tokuraku@muroran-it.ac.jp
報道に関する問い合わせ
国立大学法人室蘭工業大学総務広報課秘書広報係
Tel:0143-46-5008
E-mail:koho@muroran-it.ac.jp mailto:koho@muroran-it.ac.jp

本プレスリリースは発表元企業よりご投稿いただいた情報を掲載しております。
お問い合わせにつきましては発表元企業までお願いいたします。
お問い合わせにつきましては発表元企業までお願いいたします。
